Beth Schafer était allongée sur un lit d'hôpital, attendant la naissance de son fils. Les premières contractions étaient arrivées avant qu'elle ne se sente prête, et elle avait senti avec l'instinct profond d'une mère que son bébé n'était pas prêt non plus.
À seulement 23 semaines, son fils se trouvait à la limite de la viabilité – ce point fragile où la médecine moderne peut éventuellement maintenir un bébé en vie.
À sa naissance, si petit qu'il tenait dans une main, il n'avait pas crié. Une équipe en tenue bleue s'était précipitée pour le réanimer, essayant de remplir d'air ses petits poumons sous-développés. Mais malgré leurs efforts, ils n'avaient pas pu lui donner ce dont il avait le plus besoin : plus de temps dans l'utérus.
Beth est une peintre de 39 ans devenue graphiste. Avec ses lunettes rondes et sa frange sombre ébouriffée, elle ressemble à une étudiante en art qui n'aurait jamais quitté l'atelier. C'est le genre de personne qui vous propose du thé avant même que vous ne le demandiez, et quand elle dit "Je trouve ça génial pour toi", elle le pense sincèrement. C'est pourquoi je sais qu'elle n'exagère pas quand elle parle de son fils parfait et précieux.
« J'aurais déplacé des montagnes pour lui », m'a confié Beth, deux ans après sa naissance.
Partout dans le monde, des scientifiques travaillent pour gagner plus de temps pour les bébés extrêmement prématurés comme celui de Beth. En 2017, des chercheurs de Philadelphie ont présenté un utérus artificiel expérimental conçu pour soutenir la gestation en dehors du corps.
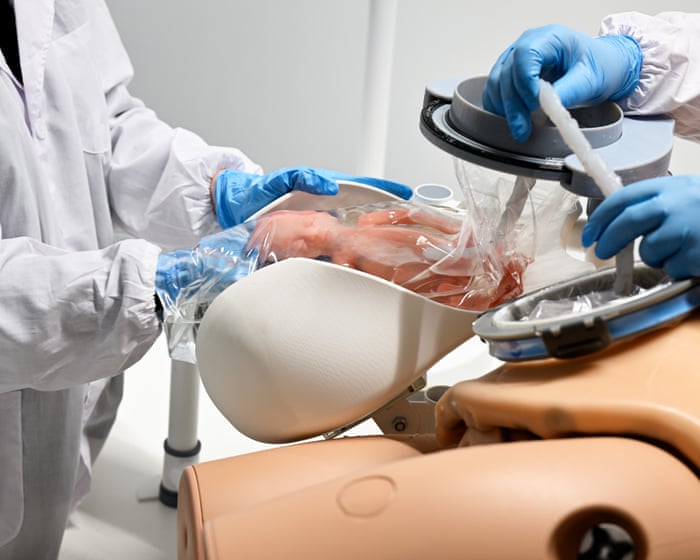
Sur les photos de leur étude, des fœtus d'agneaux flottaient paisiblement à l'intérieur de ce qui ressemblait à des sacs plastiques surdimensionnés, les yeux fermés et le cœur battant comme s'ils étaient encore dans le ventre de leur mère. Bien que l'appareil n'ait été testé que sur des animaux, il se rapproche d'essais sur l'homme.
En septembre 2023, la Food and Drug Administration américaine a rencontré un comité consultatif pour discuter de l'approbation des premiers essais cliniques sur l'homme. S'ils sont approuvés, les premiers participants seraient des bébés nés entre 22 et 24 semaines – soit moins des deux tiers d'une grossesse à terme. (La FDA a refusé de commenter la date éventuelle de début de ces essais ou même leur tenue.)
Aux États-Unis, plus de 10 000 nourrissons naissent aussi prématurément chaque année. La prématurité est la deuxième cause de mortalité infantile dans le pays, et ceux qui survivent font souvent face à de graves complications, allant de maladies pulmonaires chroniques à des problèmes neurologiques à vie.
Les utérus artificiels pourraient changer la donne, en sauvant plus de bébés et en épargnant aux familles des déchirements. Mais faire grandir un enfant en dehors du corps remet également en cause notre conception de la grossesse et de la parentalité.
« Ce type d'appareil créerait un nouveau stade de développement humain, quelque chose que nous n'avons jamais eu à décrire ou à réglementer auparavant », explique Elizabeth Chloe Romanis, spécialiste du droit médical à l'Université de Durham.
Les utérus artificiels soulèvent des questions difficiles auxquelles scientifiques, bioéthiciens et experts juridiques se confrontent avant le début des essais sur l'homme : Comment cette technologie changera-t-elle notre façon de préserver la vie, ou même notre définition de la vie elle-même ?
Quand j'ai vu le prototype pour la première fois, il ne m'a pas fait penser à un utérus – il ressemblait plutôt à un aquarium.
Le réservoir en verre repose sur une plate-forme à hauteur de taille dans un laboratoire lumineux d'Aix-la-Chapelle, en Allemagne, dans le cadre des travaux d'AquaWomb, une start-up néerlandaise développant des dispositifs pour aider les nourrissons les plus petits et les plus malades.
D'environ la taille d'un aquarium domestique, le récipient est placé sous des lumières fluorescentes pour que les techniciens puissent observer l'intérieur, bien qu'en pratique il serait couvert pour imiter l'obscurité de l'utérus. Des tubes partent des côtés vers des filtres qui font circuler un liquide amniotique synthétique selon un rythme régulier.
La conception semble adaptée aux nourrissons extrêmement prématurés, qui souvent à la naissance semblent appartenir à un autre monde – leur peau est translucide et délicate. Avec des membres fins comme des allumettes, ces bébés pourraient flotter, boire, uriner et grandir à l'intérieur du réservoir sans jamais toucher l'air.
Myrthe van der Ven, médecin technique et PDG d'AquaWomb, me montre comment leur prototype recrée l'environnement protégé de la grossesse. Le liquide amniotique est maintenu à 37,6°C, légèrement plus chaud que la température centrale d'une mère. Un sac à double paroi est suspendu au centre du réservoir. La poche intérieure se dilate à mesure que le bébé grandit, passant de la taille d'une grenade à 23 semaines à celle d'une aubergine à 28 semaines. La couche externe en silicone est plus ferme, suffisamment flexible pour résister aux coups de pied du bébé et l'aider à étirer et renforcer ses muscles.
Van der Ven explique que le réservoir est la partie facile – le vrai défi réside dans les poumons.
Lors d'un accouchement typique, la première respiration d'un nouveau-né déclenche l'instinct de respirer, souvent marqué par un cri qui montre que les poumons fonctionnent. Mais pour les bébés extrêmement prématurés, ce moment arrive trop tôt. Leurs poumons sous-développés ne peuvent même pas produire un murmure, et encore moins fournir assez d'oxygène pour soutenir le cerveau et le corps en croissance.
Dans les unités de soins intensifs néonatals actuelles, les médecins interviennent après la naissance, utilisant des ventilateurs et des couveuses pour aider ces organes fragiles à fonctionner. Mais ce soutien mécanique comporte des risques de lésions durables. Une fois que les poumons sont exposés à l'air, ils sont activés définitivement – comme un poisson qui ne peut retourner dans l'eau.
Les utérus artificiels visent à éviter entièrement cette crise. Dans la conception d'AquaWomb, le bébé est accouché par césarienne dans une poche remplie de liquide, passant de manière transparente de la mère à la machine. À l'intérieur de la chambre de transfert, les médecins reconnectent le cordon ombilical à un placenta artificiel – un dispositif de la taille d'un poing équipé de cathéters délicats pour éliminer le dioxyde de carbone du sang et de canules robustes pour délivrer oxygène et nutriments.
En cas de succès, le placenta fournit le temps que les poumons du bébé ne sont pas prêts à assumer. S'il échoue, le bébé n'a que deux minutes avant qu'un manque d'oxygène ne cause des lésions cérébrales permanentes. Tout au long de ce processus, le bébé reste immergé dans le liquide, inconscient de sa propre naissance.
« C'est comme jongler avec dix balles », explique Frans van de Vosse, professeur de biomécanique cardiovasculaire à l'Université de technologie d'Eindhoven qui conseille le projet. « Sauf que les balles sont en feu, et en faire tomber une n'est pas une option. »
S'il est perfectionné, un utérus artificiel pourrait redéfinir les limites de la survie. C'est peut-être pourquoi les quelques laboratoires développant une telle technologie sont prudents sur la façon de la nommer.
AquaWomb qualifie son prototype de « système de support vital imitant l'utérus », évitant le terme chargé d'« utérus artificiel ». Pendant ce temps, le Children's Hospital of Philadelphia (CHOP), considéré comme le plus proche des essais sur l'homme, appelle le sien un « biobag ». CHOP a fait les gros titres en 2017 lorsque des chercheurs ont maintenu en vie des fœtus d'agneaux pendant 28 jours, démontrant qu'un utérus artificiel pouvait soutenir la circulation sanguine et le développement des organes chez un animal vivant.
L'ensemble du domaine opère dans un épais secret. CHOP a décliné toute demande de commentaire pour cet article. (Vitara Biomedical, la société qui a licencié la technologie de CHOP, a levé plus de 125 millions de dollars, suggérant des préparatifs pour des essais cliniques.) Certains chercheurs ont mentionné que les scientifiques de CHOP avaient accepté de collaborer avant de se rétracter.
Cette prudence reflète à la fois l'examen minutieux autour des technologies de reproduction et la compréhension que, comme le dit van der Ven, « en science, il y a de l'évolutionnaire et du révolutionnaire ». Un utérus artificiel serait ce dernier.
Son équipe ne cherche pas à être la première à tout prix. « Nous n'avons pas besoin d'être les premiers. Nous voulons être les meilleurs », explique-t-elle. Pour elle, cela signifie concevoir un système où les parents peuvent interagir avec leur bébé en développement – une priorité essentielle. Elle estime que d'autres chercheurs ont négligé cet aspect. Une conception d'AquaWomb comporte des ports d'accès pour que les parents puissent toucher leurs bébés. Une autre inclut un « téléphone utérin » qui diffuse des voix, de la musique ou des battements de cœur dans le liquide au même volume étouffé qu'un fœtus entendrait dans l'utérus.
Ces interactions – toucher un petit pied, parler dans le liquide, sentir les mouvements à l'intérieur du sac – pourraient améliorer la santé à long terme des nourrissons prématurés. Mais l'importance du lien pendant la grossesse va au-delà des taux de survie.
Des études sur les familles utilisant la FIV ou la gestation pour autrui montrent que lorsque la grossesse ne suit pas le chemin habituel, les parents – surtout les mères – peuvent avoir du mal à se sentir comme de vrais parents. Les naissances très prématurées peuvent déclencher des émotions similaires, en partie parce que la prématurité découle souvent de problèmes médicaux chez la mère, et non chez le bébé.
« Ils pourraient avoir l'impression de ne pas avoir rempli leur devoir de protection et de portage de leur enfant », dit Romanis. Elle estime que toute alternative éthique à la grossesse naturelle doit soutenir les besoins émotionnels des parents autant que les besoins physiques du bébé.
En bref, voir son bébé flotter dans un réservoir ou enfermé dans un sac pourrait changer non seulement la façon dont on crée des liens avec lui, mais aussi la façon dont on se perçoit en tant que parent.
Trois mois après avoir perdu son fils, Beth a rejoint un groupe de soutien qui se réunit deux fois par mois pour les parents ayant perdu un bébé tard dans la grossesse ou peu après la naissance, souvent à cause d'une extrême prématurité. Ils parlent de ce qu'il faut faire des cadeaux pour bébé non utilisés ou comment gérer les questions de la famille et des collègues. Beaucoup ont eu des enfants qui auraient pu être des candidats idéaux pour un utérus artificiel.
Quand Beth m'a invitée, j'ai imaginé un amphithéâtre ou une salle de réunion d'hôpital. Au lieu de cela, nous nous sommes rencontrés dans le sous-sol d'une église de Boston, où Wendy, la thérapeute qui anime le groupe, avait installé un cercle de chaises pliantes. Les gens arrivaient lentement.
Parmi les 17 participants aujourd'hui, un seul était un homme – lui et son mari ont perdu leur fille lorsque leur mère porteuse a fait une fausse couche tardive. En face de moi était assise une fille qui semblait trop jeune pour commander un verre, et encore moins pour avoir eu et enterré un bébé. Ses cheveux blonds décolorés effleuraient les cheveux poivre et sel de Joanne ; Joanne, presque 60 ans, vient depuis trois ans, ayant rejoint le groupe plus de dix ans après la perte de son fils. Le groupe comprend également une professeure d'anglais, une mère au foyer, un policier et une infirmière pédiatrique.
Dans ce cercle, il est clair que la perte d'une grossesse affecte les gens de manière inégale, mais le chagrin les touche tous également.
Personne ne sait depuis combien de temps le groupe existe. Les gens en entendent parler par le bouche-à-oreille. « Nous avons essayé de créer un groupe Facebook une fois », m'a dit Beth, « mais il a été envahi par des anti-vaccins demandant si nous avions reçu le vaccin Covid. »
« Et puis mon compte a été suspendu parce que je leur ai dit d'aller se faire voir », a ricané Joanne. « Quand j'ai perdu mon bébé, j'ai aussi perdu ma patience pour gérer des adultes attardés. »
Wendy a posé une main sur le poignet de Joanne et m'a fait un clin d'œil. « Comme vous pouvez le voir, nous sommes très ouverts ici. Vous pouvez nous interroger sur vos sacs à bébé. »
« Biobags », ai-je corrigé entre des rires saccadés, surprise par leur décontraction. J'ai expliqué que la technologie est encore à des années des hôpitaux et ne serait probablement proposée qu'aux nourrissons nés à 22 ou 23 semaines, qui n'ont guère d'autres options.
« J'ai perdu mon bébé à 22 semaines », a coupé Joanne. « Vous dites que cela aurait pu le sauver ? »
« Peut-être », ai-je admis. « Mais pas certainement. Hypothétiquement, si vos médecins avaient pensé qu'il était candidat pour un utérus artificiel, auriez-vous… »
« Absolument », a insisté Joanne. « Je ne voulais que le sauver. Si mon corps ne pouvait pas le faire, alors peut-être que ce truc d'utérus aurait pu. »
Les parents sont avides de la moindre information pour nourrir leurs « Et si ? » : Et si mon bébé avait pu survivre à 21 semaines ? Combien cela aurait-il coûté ? Aurais-je pu voir ma fille, la tenir ?
Quand je décris les prototypes, deux femmes grimacent, mais les autres se penchent, demandant des photos. Ils imaginent leurs enfants dans un utérus artificiel, flottant paisiblement dans un état semblable à un rêve.
Ces parents ne savent pas exactement ce que la technologie aurait pu offrir, mais ils ressentent profondément ce qu'ils ont perdu sans elle. La plupart n'ont pas démonté les lits de leurs bébés. L'infirmière pédiatrique pense à changer de métier parce qu'être près des nouveau-nés lui donne envie de pleurer. Beth se tient souvent le ventre en parlant, comme si elle berçait un enfant qui n'est pas là.
Chaque parent est hanté par l'idée de ce qu'il aurait pu faire de plus. Beaucoup croient que plus d'intervention, plus de technologie, aurait pu sauver leurs bébés.
Wendy fait une pause. « Est-ce que plus est toujours mieux ? » Elle se souvient avoir accouché de sa fille par césarienne à 24 semaines et avoir supplié les médecins pour des soins intensifs. Malgré la naissance risquée, ils ont sauvé le bébé en salle d'opération, pompant manuellement sa poitrine pour faire circuler le sang vers son cerveau. Pendant quatre mois en soins intensifs néonatals, sa fille a été branchée à des tubes et a reçu des médicaments. Les procédures étaient coûteuses et douloureuses, mais ses poumons sous-développés avaient besoin de plus de temps pour se développer.
Wendy aussi avait besoin de plus de temps. « Le pronostic était sombre, mais quand c'est votre enfant, vous continuez d'espérer un miracle. Je ne pouvais pas la laisser partir. »
Après 131 jours, sa fille est morte d'un poumon collapsé. Pendant des mois, Wendy a été consumée par la culpabilité, son chagrin coulant chaud et salé sur ses joues. « Je me sentais si égoïste », dit-elle. « Même si j'ai dépassé ces sentiments, j'aurais souhaité lui offrir une fin plus paisible, plus courte. »
Bien qu'elle soutienne le développement des utérus artificiels, Wendy se demande comment les médecins obtiendront un consentement véritablement éclairé de parents désespérés. « Peut-être qu'à l'